 |
| International Society of Pharmacovigilance-Indonesia Chapter, Evi Dwi Noviarny membahas pengalaman ISoP untuk mendorong budaya pelaporan dan meningkatkan kualitas data laporan efek samping. |
OMAIdigital.id- Farmakovigilans merupakan aktivitas untuk mendeteksi dan mencegah efek samping obat, termasuk efek samping dari OBA, OK, dan SK. Maka Farmakovigilans menjadi faktor kunci dari perlindungan masyarakat, mengingat efek samping atau kejadian tidak diinginkan (KTD) seringkali baru terdeteksi setelah produk beredar.
Bahkan, Farmakovigilans dapat menjadi tools yang berguna untuk mengidentifikasi penyebab kejadian luar biasa (KLB) agar dapat dilakukan tindak lanjut secara cepat.
Beberapa kasus di Indonesia maupun dunia menunjukkan bagaimana laporan efek samping dapat menyelamatkan masyarakat. Misalnya, pada kasus Ephedra di tahun 2004, yang menyebabkan Ephedra akhirnya dilarang beredar karena terbukti menimbulkan risiko toksik pada jantung hingga menimbulkan kematian.
Terkait dengan urgensi Farmakovigilans, BPOM menggandeng World Health Organization (WHO) menyelenggarakan Workshop on Implementation of Adverse Effect Monitoring of Herbal Medicines and Health Supplements.
Kegiatan ini berlangsung pada 28-29 Agustus 2025 di Jakarta dengan melibatkan perwakilan person in charge (PIC) farmakovigilans dari seluruh unit pelaksana teknis (UPT) BPOM di Indonesia sebagai peserta pelatihan.
Kepala BPOM, Taruna Ikrar memberi apresiasi kepada WHO atas dukungan dan kerja sama dalam penguatan kapasitas pengawasan farmakovigilans di bidang obat bahan alam (OBA), obat kuasi (OK), dan suplemen kesehatan (SK).
Taruna menegaskan pentingnya pelatihan ini sebagai upaya untuk deteksi dini efek samping yang mungkin timbul dari produk OBA dan SK yang beredar.
"Seiring meningkatnya tren penggunaan OBA dan SK oleh masyarakat, kebutuhan jaminan keamanan, mutu, dan khasiat produk juga semakin tinggi. Sistem pemantauan efek samping menjadi pilar penting dalam pengawasan produk tersebut," jelas Taruna Ikrar seperti dikutip di laman web BPOM.
WHO yang menjadi mitra utama BPOM dalam pelaksanaan pelatihan hari ini menyampaikan apresiasi atas komitmen BPOM dalam menjaga keamanan produk kesehatan. Team Lead Health System WHO Indonesia Roderick Salenga, saat menyampaikan sambutannya, menyampaikan bahwa surveilans yang efektif sangat penting untuk memastikan produk yang beredar tetap aman dan bermutu tinggi.
"Kami mendorong semua peserta untuk aktif berdiskusi dan menerapkan ilmu yang diperoleh dalam kegiatan ini," tutur Roderick.
Berbagai Narasumber Kompeten
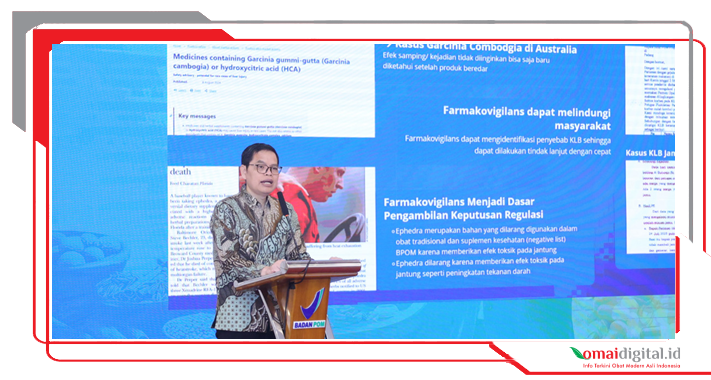
Workshop ini menghadirkan sesi paparan dan diskusi bersama narasumber dari berbagai lembaga nasional dan internasional.
Deputi Bidang Pengawasan Obat Tradisional, Suplemen Kesehatan, dan Kosmetik BPOM, Mohamad Kashuri mempresentasikan materi "Farmakovigilans OBA, OK, dan SK di Indonesia".
Kashuri menekankan urgensi pelaporan farmakovigilans, khususnya pada OBA yang memiliki komposisi lebih kompleks dibandingkan obat modern.
"Farmakovigilans menjadi dasar pengambilan keputusan regulasi. Dengan sistem pelaporan yang terintegrasi dan responsif, kita dapat meminimalisir dampak yang merugikan masyarakat," jelas Mohamad Kashuri.
Workshop kali ini dirancang untuk memberikan pemahaman komprehensif kepada PIC UPT BPOM mengenai prinsip farmakovigilans, mekanisme pelaporan, serta praktik internasional terbaik.
Agenda hari pertama diisi dengan paparan dari beberapa narasumber. Materi pertama dibawakan oleh Guru Besar Farmakologi dan Terapi Universitas Indonesia, Purwantyastuti yang membahas tentang pengertian dan pentingnya efek samping OBA, obat kuasi, dan SK di Indonesia.
International Society of Pharmacovigilance (ISoP)-Indonesia Chapter, Evi Dwi Noviarny pada event ini membahas pengalaman ISoP dalam mendorong budaya pelaporan dan meningkatkan kualitas data laporan efek samping OBA, OK, dan SK.
Technical Officer (Traditional Medicine)-WHO Regional Office for the Western Pacific, Eileen Eunkyung Han yang memaparkan tentang best practices dan tantangan dalam farmakovigilans herbal.
Materi hari pertama diakhiri dengan sharing session bersama narasumber dari BPOM. Hal yang dibahas dalam diskusi yaitu pengawasan penerapan farmakovigilans di industri farmasi, juga tentang peran dan kolaborasi PIC UPT dalam sistem monitoring efek samping OBA, OK, dan SK.

Hari kedua workshop akan dilanjutkan dengan kunjungan lapangan (inspection visit) ke beberapa industri farmasi dan obat tradisional. Kunjungan ini bertujuan melihat langsung implementasi pelaksanaan monitoring efek samping di Industri.
BPOM berkomitmen untuk terus membangun sistem farmakovigilans yang transparan, berbasis bukti, dan dipercaya masyarakat. Melalui kegiatan ini, BPOM berharap agar seluruh PIC mampu mengimplementasikan pemantauan efek samping secara konsisten sehingga keamanan, khasiat, dan mutu produk OBA, OK, dan SK senantiasa terjamin.
BPOM bersama mitra internasional juga akan terus memperkuat kolaborasi strategis untuk menciptakan ekosistem pengawasan yang lebih adaptif, modern, dan terintegrasi.
Melalui kesempatan ini, BPOM menegaskan bahwa pemantauan efek samping bukan hanya menjadi kewajiban regulator, melainkan langkah strategis bersama untuk melindungi masyarakat dari risiko sebelum produk digunakan secara luas. Peran serta masyarakat juga sangat diperlukan untuk mengoptimalkan pelaksanaan dan fungsi dari sistem farmakovigilans di Indonesia.
"Pelaporan dari masyarakat sangat penting. Tanpa data yang lengkap, sulit bagi regulator untuk mendeteksi dini potensi bahaya. Mari kita jadikan pelaporan KTD sebagai budaya bersama demi keselamatan kita semua," pesan Kepala BPOM. Redaksi OMAIdigital.id
































